Comment les cellules sont influencées par leur environnement lors de la croissance des tissus
Résumé
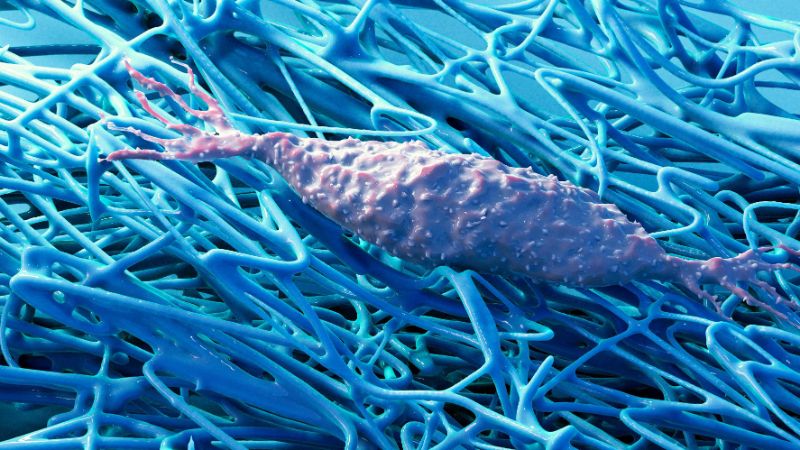
- Un nouveau système de culture tissulaire est utilisé pour cultiver non seulement des cellules humaines mais aussi la matrice fibreuse naturelle qui les entoure.
- Les cellules et cette matrice fibreuse interagissent réciproquement, notamment pour contrôler la croissance des tissus.
- À l'avenir, ces cultures de tissus seront utilisées pour tester de nouvelles substances actives, évitant ainsi le recours à l'expérimentation animale.
- Les nouvelles découvertes pourraient aider le domaine de la mécanomédecine à développer de nouvelles thérapies contre la fibrose et le cancer.
Comment un embryon se développe-t-il ? Comment les enfants grandissent-ils, comment les blessures se cicatrisent-elles ou comment le cancer se propage-t-il ? Tout cela est lié à la croissance des tissus corporels. L'un des principaux intérêts de recherche de Viola Vogel, professeure à l'ETH Zurich, et de son assistant Mario C. Benn, est de comprendre cette croissance en détail. Dans leur quête, il et elle se sont écarté·es des sentiers battus de la recherche. Pendant longtemps, la biologie a consisté à étudier les cellules et la biochimie des processus métaboliques qui s'y déroulent, souvent sans tenir compte de leur environnement naturel. Viola Vogel et Mario C. Benn, en revanche, se concentrent sur la matrice extracellulaire (MEC), une structure fibreuse qui entoure les cellules du corps. Cette matrice est produite par les cellules elles-mêmes et constitue un composant majeur de tous les tissus.
Il existe de nombreuses interactions différentes entre les cellules du corps et cette matrice fibreuse. Ces dernières années, la recherche a de plus en plus montré que toutes ces interactions ne sont pas exclusivement biochimiques. En fait, certaines sont mécaniques ou physiques. Par exemple, les cellules sont capables de détecter des stimuli mécaniques provenant de cette matrice extracellulaire.
Avec leur équipe de recherche, Viola Vogel et Mario C. Benn ont maintenant pu reproduire la croissance des tissus in vitro et étudier ce processus en détail. «Nos résultats soulignent l'importance des interactions entre les cellules et la matrice extracellulaire», déclare Mario C. Benn. À terme, il espère pouvoir utiliser ces résultats à des fins médicales, par exemple pour prévenir les troubles de la cicatrisation ou pour traiter le cancer et les maladies du tissu conjonctif.
Transformation cellulaire
Leur étude a porté sur deux types de cellules : les fibroblastes et les myofibroblastes. Chacun d'entre eux est important pour la fonctionnalité des tissus humains, et chacun peut se transformer en l'autre. Les fibroblastes se trouvent dans le tissu conjonctif de nos organes, où ils veillent à ce que la matrice extracellulaire soit continuellement renouvelée et reste saine. En cas de blessure ou de besoin de croissance tissulaire, les fibroblastes se transforment en myofibroblastes, qui jouent un rôle clé dans la cicatrisation des blessures et la croissance de nouveaux tissus. Les myofibroblastes produisent non seulement de grandes quantités de MEC, mais sont également suffisamment forts pour, par exemple, rassembler les tissus dans les plaies.
«Lorsqu'il s'agit de cicatrisation, les myofibroblastes sont nos amis», explique Marius C. Benn. Cependant, une fois leur travail terminé, il est important que ces myofibroblastes se transforment à nouveau en fibroblastes, moins actifs. Si ce n'est pas le cas, cela peut entraîner une fibrose, c'est-à-dire la formation excessive de tissu cicatriciel. Les myofibroblastes sont également présents dans les tissus cancéreux. Pour de nombreux cancers, un taux élevé de ces cellules est associé à un mauvais pronostic.
Matrice tridimensionnelle
On sait un certain nombre de choses sur les processus biochimiques qui ont lieu lorsque les myofibroblastes se transforment en fibroblastes. Cependant, peu de recherches ont été menées pour expliquer l'influence de la MEC sur cette transformation cellulaire. «Avec les méthodes conventionnelles de culture cellulaire, les cellules se développent à plat sur la boîte de culture. Cela conduit à la formation d'une MEC non naturellement plane», explique Viola Vogel. «De toute façon, jusqu'à présent, la recherche a généralement ignoré la MEC. Mais étudier les cellules sans la matrice extracellulaire, c'est un peu comme étudier le comportement des araignées sans leur toile».
La méthode utilisée par Viola Vogel et Mario C. Benn est très différente. Elle a été développée à l'origine à l'Institut Max Planck des colloïdes et interfaces de Potsdam et a été affinée par les scientifiques de l'ETH Zurich. Ils et elles utilisent un échafaudage en silicone, enduit de protéines spécifiques, qui présente des fentes microscopiques en forme de triangle et repose dans un milieu de culture tissulaire. Sur une période de deux semaines, de nouveaux tissus se forment dans ces fentes, en même temps qu'une MEC plus naturelle. La croissance commence à l'apex, remplissant progressivement la fente au fur et à mesure que le tissu se développe.
Les chercheurs et chercheuses ont observé que les myofibroblastes sont toujours situés précisément sur le front de croissance, c'est-à-dire dans la zone du tissu qui est en train de se former. Elles et ils ont également pu montrer comment les myofibroblastes de cette zone forment une nouvelle MEC - d'abord sous une forme provisoire, puis sous une forme plus stable - avant de se reconvertir en fibroblastes. «Ces processus sont similaires à ceux qui ont lieu dans le tissu sous-cutané humain pendant la phase tardive de la cicatrisation des plaies», explique Mario C. Benn.
Les scientifiques ont également pu montrer que l'évolution rapide de la MEC est l'un des déclencheurs de la réversion des myofibroblastes en fibroblastes. De plus, cette réversion est favorisée lorsqu'un certain type de fibre de la MEC - la fibronectine - passe d'un état étiré à un état détendu. Il semble probable que des processus interactifs similaires se produisent lors de la cicatrisation des plaies.
Les chercheurs et chercheuses ont ensuite volontairement interféré avec la transition cellulaire en utilisant divers agents qui modifient la composition ou la structure de la matrice extracellulaire. Ils et elles ont ainsi pu reproduire ce qui se produit dans des pathologies telles que la fibrose ou le cancer, à savoir qu'au lieu de redevenir des fibroblastes comme dans les tissus sains, les myofibroblastes sont stabilisés par la matrice extracellulaire.
La mécanomédecine du futur
Les chercheuses et chercheurs espèrent que ces cultures de tissus miniatures les aideront à déchiffrer les détails de l'interaction entre les cellules humaines et leur matrice extracellulaire. Cette méthode permettra non seulement d'éviter les tests sur les animaux, qui sont souvent nécessaires dans la recherche biomédicale, mais elle pourrait également être utilisée à l'avenir pour tester des substances candidates lors de la mise au point de médicaments. «Ces applications et ces questions de recherche sont très prometteuses», explique Mario C. Benn. «Si nous parvenons à comprendre comment les myofibroblastes et les fibroblastes se transforment les uns en les autres et à contrôler ce processus, nous pourrons également faire des progrès considérables dans des domaines tels que les troubles de la cicatrisation des plaies, la fibrose et le cancer.
Viola Vogel et Mario C. Benn évoquent également un domaine d'avenir appelé mécanomédecine. Ce terme décrit l'application médicale des résultats obtenus dans le domaine de la mécanobiologie : l'étude de la façon dont les cellules peuvent détecter et traiter les signaux mécaniques. En d'autres termes, la mécanomédecine vise à appliquer les connaissances acquises en mécanobiologie à la pratique médicale.
À terme, les scientifiques espèrent utiliser la mécanomédecine dans le développement de nouvelles méthodes de diagnostic pour la détection précoce des tissus fibrotiques. «Dans de nombreuses pathologies, dont la fibrose pulmonaire, la réussite du traitement dépend de la détection précoce», explique Mario C. Benn. Les méthodes de dépistage actuelles ne permettent pas de détecter les myofibroblastes dans les tissus pulmonaires avec une grande précision. Le chercheur espère maintenant qu'une étude plus approfondie de la matrice extracellulaire révélera des biomarqueurs permettant une détection plus précoce et plus facile de la fibrose et d'autres maladies similaires du tissu conjonctif.